Nuove evidenze sull’evoluzione dei virus
Uno studio internazionale ha indagato la struttura e l’assemblaggio di un “contenitore” composto da un enzima batterico per comprendere l’evoluzione dei virus in un sistema artificiale. I risultati, pubblicati su Science, descrivono un processo che potrebbe essersi verificato nella prima evoluzione dei virus
L’origine dei virus non è chiara. Nel corso degli anni, sono state formulate molte ipotesi per spiegare la storia evolutiva di questi “organismi ai margini della vita”; tuttavia, ad oggi, nessuna di esse è stata confermata.
I virus sono entità biologiche eterogenee costituite da un rivestimento proteico esterno, il capside, che contiene e protegge il genoma virale. Questa struttura prende il nome di nucleocapside e ha una forma, una dimensione e una simmetria definite. Ricreare queste caratteristiche in un contenitore non virale per studiare l’evoluzione dei virus in un sistema artificiale, è stata la sfida di un team di ricercatori del Politecnico federale di Zurigo, in collaborazione con le università di Leeds e York.
A partire da una delle teorie sull’evoluzione dei virus, che afferma che i primi progenitori virali si siano serviti di proteine ospiti per la formazione del virione (termine con cui si indica una singola particella virale), il team di ricerca ha utilizzato, come contenitore virus-like, un enzima estratto dal batterio Aquifex aeolicus. Per prima cosa, gli autori hanno convertito l’enzima in un nucleocapside artificiale in grado di legare il proprio Rna messaggero (mRna) per studiarne la struttura, l’assemblaggio e l’evoluzione nel tempo.
Gli autori hanno osservato una trasformazione strutturale a carico del nucleocapside rispetto alla conformazione di partenza; il contenitore artificiale, infatti, si è riorganizzato in una struttura in grado di impacchettare in maniera più efficiente il proprio mRna. Nel dettaglio, gli studiosi hanno rilevato un’espansione del diametro del contenitore per accogliere meglio l’mRna, e un ridimensionamento dei pori presenti sulla sua superficie per proteggere il materiale genetico dalle nucleasi (enzimi presenti nelle cellule che tagliano i legami che compongono un acido nucleico).
Per osservare questi cambiamenti strutturali, i ricercatori hanno utilizzato la tecnica della microscopia crioelettronica, un tipo di microscopia elettronica messa a punto nell’ultimo ventennio da tre scienziati, Jacques Dubochet, Joachim Frank e Richard Henderson, che consente di osservare un campione biologico nel suo ambiente nativo con una risoluzione che raggiunge i singoli atomi. La tecnologia consiste nel congelare il campione e bombardarlo con un fascio di elettroni in modo da ottenere un’istantanea delle strutture tridimensionali di biomolecole molto piccole, come le proteine di rivestimento dei virus, senza doverle colorare o fissare, come accade con le tecniche di microscopia elettronica tradizionali. Per aver rivoluzionato il mondo della microscopia, i tre scienziati hanno vinto il premio Nobel per la chimica nel 2017.

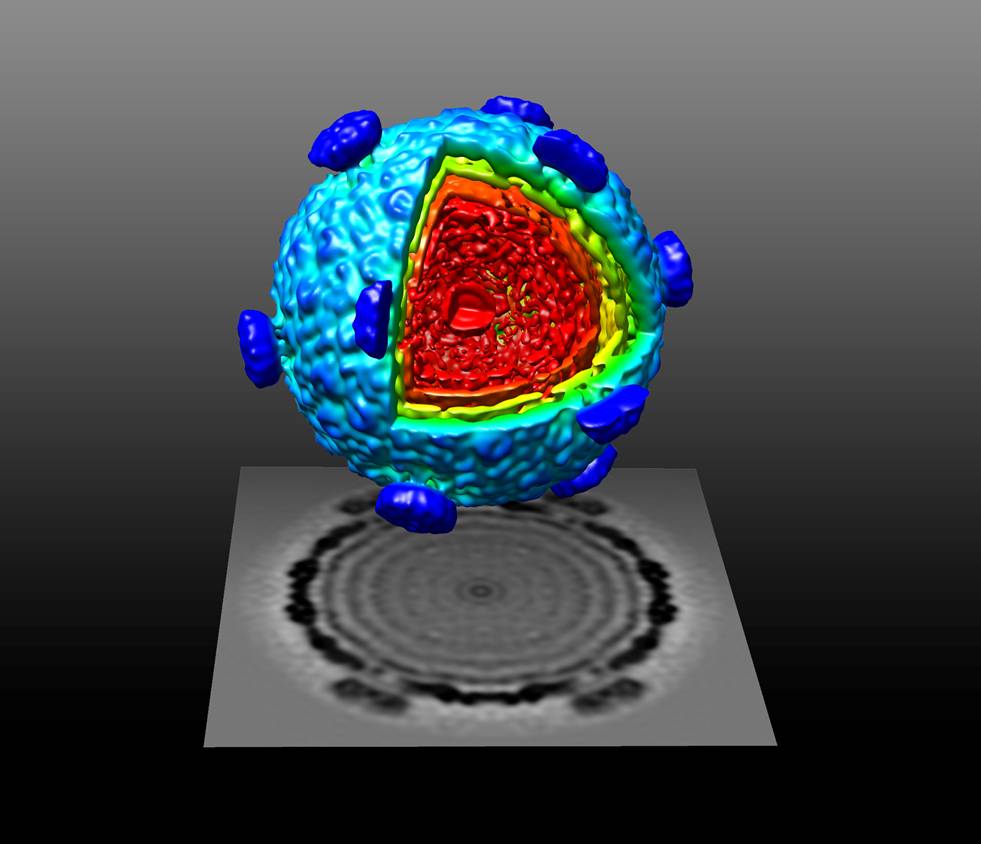
Ma torniamo allo studio. Resta una domanda importante da porsi: cosa ha guidato la trasformazione strutturale del nucleocapside per rendere l’impacchettamento del proprio mRna più efficiente? La risposta risiede nel mRna stesso. Esistono, infatti, particolari regioni nel genoma dei virus che contengono dei “segnali” che guidano la particella virale a impacchettare in modo corretto e specifico il materiale genetico nel capside. Questo meccanismo è ampiamente usato dai virus naturali, tra cui il Covid-19. In questo studio, è stato visto che l’mRna presente nel contenitore virus-like evolve proprio questi “segnali”; ciò significa che un sistema artificiale ha evoluto lo stesso processo presente nei virus naturali. Questa scoperta rivela un meccanismo evolutivo che potrebbe essersi verificato nei virus primordiali e apre la strada all’utilizzo dei costrutti artificiali come valida alternativa agli agenti patogeni naturali, per lo sviluppo di nuove strategie terapeutiche.
Immagine in evidenza: virus Zika {Wikimedia commons}















Commenti recenti